FINCH1試験の試験概要と 有効性・安全性の結果
FINCH1試験は、MTXで効果不十分な中等度から重度の活動性関節リウマチ患者を対象に、
MTX併用下で52週間フィルゴチニブを投与した時の有効性と安全性を検討した国際共同第III相検証試験であり、
多施設共同、無作為化、二重盲検、プラセボ及び実薬対照、並行群間比較試験です。
この動画では、産業医科大学医学部第1内科学講座教授 田中良哉先生に、FINCH1試験の概要および有効性・安全性の結果を解説していただきます。

FINCH1試験:試験概要
FINCH1試験は、MTXで効果不十分な中等度から重度の活動性関節リウマチ患者を対象に、MTX併用下で52週間ジセレカを投与した時の有効性と安全性を検討しました。対象患者は1755例で、このうち147例が日本人でした。

FINCH1試験:試験デザイン
ジセレカ200mg群、100mg群、アダリムマブ群、プラセボ群に無作為に割り付け、52週まで投与しました。プラセボ群は投与24週時にジセレカ200mg群または100mg群に1:1の比率で再無作為化し、投与52週時まで試験を継続しました。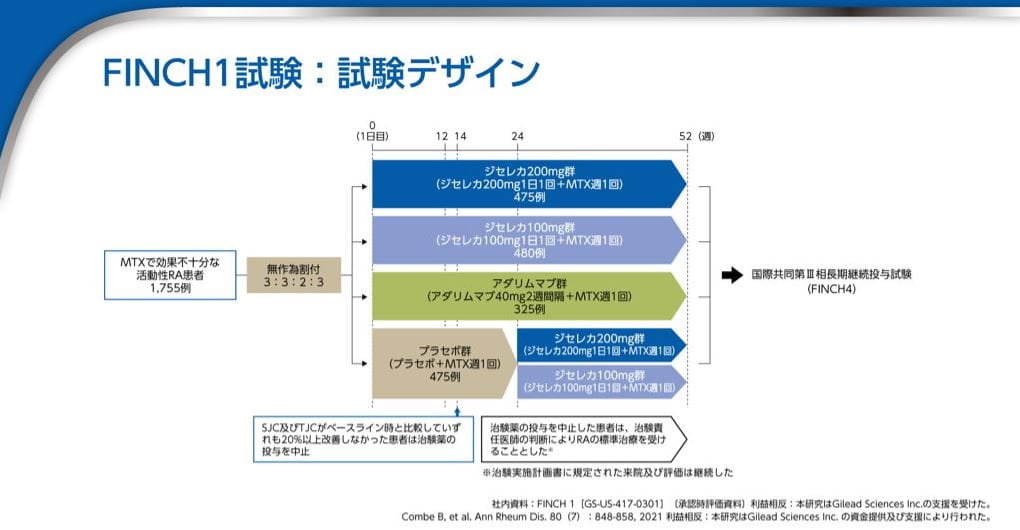
- 演者
- 産業医科大学医学部第1内科学講座 教授
田中 良哉 先生
目次
試験概要
- 試験概要【00:00】
有効性
- 投与12週時のACR20改善率、投与24週時のmTSSのベースラインからの変化量(主要評価項目〔検証的評価項目〕)【07:22】
- ACR20/50/70改善率の推移(副次評価項目)【09:00】
- 投与52週時のmTSSのベースラインからの変化量、投与24・52週時のX線所見で進行がみられない患者割合 (副次評価項目)【11:27】
- 投与12週時および投与24週時のDAS28(CRP)≦3.2達成率、SDAI≦11.0達成率、CDAI≦10.0達成率による低疾患活動性の各指標の達成率(副次評価項目・追加された評価項目)【13:18】
- 投与24・52週時のDAS28(CRP)<2.6達成率、SDAI≦3.3達成率、CDAI≦2.8達成率、Boolean基準による寛解達成率(副次評価項目・追加された評価項目)【15:23】
- HAQ-DIのベースラインからの変化量(副次評価項目)【17:29】
安全性
- 投与52週までの安全性 有害事象の概要【18:25】
- 投与52週までの安全性 主な有害事象【19:26】
- 投与52週までの安全性 重篤な有害事象【24:50】
- 投与52週までの安全性 投与中止に至った有害事象【31:39】
- 投与52週までの安全性 死亡に至った有害事象【36:15】
- 投与52週までの安全性 特に注目すべき有害事象【38:06】
- 日本人集団における安全性(サブグループ解析)有害事象の概要【42:06】
- 日本人集団における安全性(サブグループ解析)主な有害事象【43:07】
- 日本人集団における安全性(サブグループ解析)重篤な有害事象、投与中止に至った有害事象【47:05】
- 日本人集団における安全性(サブグループ解析)特に注目すべき有害事象【50:09】
まとめ
- まとめ【51:45】





